第一节 产品技术发展现状
国内一般采用生产技术基本如下:
选用新鲜的或冷冻保存的检疫合格动物肝脏洗净,剔除筋膜,加入一定比例的注射用水,用胶体磨匀浆,制得肝脏匀浆液。后将匀浆液冻存,反复冻融多次,破碎肝脏细胞,调节提取液邮值略中性,加热使其变性,冷却到室温,离心得上清液,最后用超滤膜超滤离心上清液,即得HCF粗品溶液。
1、提取工艺确定:
生化原料的提取破碎方法一般有机械法、冻融法、冷热交替法、超生波处理法、加压破碎法、化学法、酶处理法等几种,其中机械法.冻融法对设备环境条件要求低,并能较好地保持生化原料中天然成分的活性。有专家以胎牛肝组织为原料,分离胎肝细胞,—80℃反复冻融后匀浆,离心沉淀取上清液,用超滤法分离得中分子细胞因子(MMCF)和低分子细胞因子(LMCF),并用肿瘤细胞进行了生物效应对比 研究 。有专家也对提取过程中影响因素进行考查,确定了将新鲜小牛肝脏匀浆4次、反复冻融5次、90℃保温5rain变性、6000分子量超滤等工艺条件,最终提取率可达到1.6%。部分专家对匀浆破碎和板框过滤的条件进行了改进,将原用的胶磨机改为分散乳化机,同时滤渣再提取时,加入注射用水中,搅拌重新板框过滤,提取量可增加40%左右。
2、肝细胞生长因子的质量控制
促肝细胞生长素的国家制定的质量标准中除(性状)观察,用pH计检测(酸碱度),分光光度法(蛋白质)和HPLC法(高分子物质)、福林—酚法多肽(含量测定)、动物实验检测(异常毒性)、(降压物质)等指标。而(活力检测)检测成为质量检测的难点。
3、生物活性检测
促肝细胞生长素的疗效与其生物活性密切相关,因此其活性检测方法是质量控制的关键。由于促肝细胞生长素成分的复杂性,在检测过程中受到多种因素的制约,尤其是现阶段面临生化药物活性检测方法改良阶段,因此,寻求出高质量、高效率、特异性强、成本低、方便快捷的活性检测方法成为质量生产控制,产品质量评价和监督的重要手段。
肝细胞生长因子活性检测的经典方法是3H—TdR掺入法,因灵敏度高,特异性强,可以比较客观地量化反映包括HGF在内的增殖活性。
促肝细胞生长素质量标准是质量控制的关键,关系到产品的安全性、稳定性及有效性。由于促肝细胞生成素成分组成比较复杂,现行的质量标准检测项目比较片面,不能反映整体药效组分和生物药物特殊性,由于促肝细胞生长素基础性质量控制方面的 研究 比较少,特别是活性检测方法亟待更深入的 研究 和比较,以确保质量,最大程度上发挥药效,确保安全性。
第二节 产品工艺特点或流程
促肝细胞生长素(HGF)溶液是自健康的猪或牛类新鲜肝脏中提取的具有生物活性的多肽溶液,主要成分为HGF。
1、生产工艺
生产工艺路线为:
合格的小牛肝脏准备:取新鲜小牛肝脏,目检,表面应光滑,无任何豆状突起,色泽为粉红色。将合格的小牛肝脏盛装于洁净的塑料袋中,密封,—18℃以下冷冻保存。
新鲜小牛肝脏匀浆制备:将新鲜的小牛肝脏洗净,剔除筋膜,切成5~10cm的小块,按总量比例1:l(纯化水:肝脏)加入纯化水,在胶体磨通入冷却水的条件下,匀浆4次,得肝脏匀浆液。
匀浆液冻融提取:将匀浆液于—18℃冷冻,冻实后,室温缓慢化冻,完全融化后,再将其于—18℃冷冻,如此反复5次,破碎肝脏细胞,提取多肽。
提取液加热变性:将提取液pH值调节为6.5~7.0,水浴加热至90℃,保温5min,冷却至室温,离心,得上清液。
超滤:用截留分子量为6000的超滤膜超滤离心上清液,即得HGF溶液。
2、提取方法的确定
生化原料的提取破碎方法一般有机械法、冻融法、冷热交替法、超声波处理法、加压破碎法、化学法、酶处理法等几种,其中机械法、冻融法对设备环境条件要求较低,并能较好地保持生化原料中天然成分的活性。因此,采用了机械法和冻融法联合使用的提取方法,并对提取过程中的一些影响参数进行了比较。
匀浆次数:将切好的肝脏按总量比例1:1(纯化水:肝脏)加入纯化水,调节好胶体磨的最小间隙,匀浆,离心,取上清液测定多肽的含量,结果见下图。可见,匀浆次数越多,粉碎效果越好,多肽提取率越高;匀浆4次时多肽含量几乎达到最大,再增加匀浆次数,多肽含量几乎不再增加。因此,匀浆次数选定为4次。
匀浆次数对多肽提取率的影响
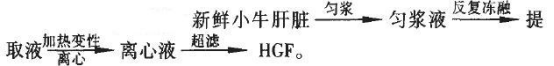
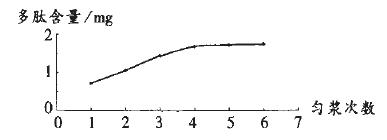
冻融次数:不同的冻融次数对多肽提取率的影响见下图。可见,冻融次数是多肽提取的一个重要因素,随着冻融次数的增加,多肽含量几乎呈直线上升;但5次冻融后,含量随冻融次数增加呈减少趋势,再增加1次冻融,多肽含量增加不大,反而会延长生产周期。因此,冻融次数选定为5次。
冻融次数对多肽提取率的影响
加水比例:纯化水与肝脏的比例分别按0.5:1,1:l,1.5:1,2:1加入纯化水,匀浆4次,冻融5次,离心取上清液,测定多肽含量,结果见下图。可见,加水比例为l:1时,多肽提取率最大;再增大加水比例,多肽含量无明显提高,反而会使溶液的浓度降低。因此,选用l:1的加水比例比较合理。
加水比例对多肽提取率的影响
3、加水比例对多肽提取率的影响
热变性主要目的是使提取液中大分子蛋白质变性沉淀而得到澄清溶液。不同温度、不同时间的变性试验结果见下表。可见,85℃保温15min,90℃保温5min以上都能达到良好的变性效果,且90℃保温5min条件下变性,保温时间短,对溶液中有效成分破坏较小。因此,选用90℃保温5min条件下变性较合理。
同温度、时间的变性试验结果
| 时间(min) | 温度(℃) | ||
| 80 | 85 | 90 | |
| 5 | 浑浊 | 浑浊 | 澄清 |
| 10 | 浑浊 | 浑浊 | 澄清 |
| 15 | 浑浊 | 澄清 | 澄清 |
4、超滤膜的选择
HGF溶液的国家药品标准中高分子物质检查项以胰岛素(分子量5800)为对照品。故选用截留分子量为6000的超滤膜进行分子截留。
5、样品 分析
采用上述工艺 研究 确定的工艺路线,在符合GMP的生产车间进行了3批样品的生产,按标准检验各项指标均符合规定,3批样品的 分析 结果见下表。对加速试验留样6个月的样品进行检验,各项指标与留样前比较无明显变化,符合标准要求。说明该工艺条件合理可行,产品质量符合要求,存放期间稳定。
3批样品质量 分析 结果

优选的工艺条件是将新鲜小牛肝脏匀浆4次、反复冻融5次、90℃保温5min变性、6000分子量超滤。通过该工艺制备的产品提取率能达到1.6%(多肽含量/肝脏),且各项指标均符合国家药品标准。该工艺制备简单,对设备要求低,适合制药企业大规模生产。
第三节 国内外技术未来发展趋势 分析
1、临床应用
促肝细胞生长素及其他同类制剂因其安全,副作用少,疗效较好等优点。大量文献报道促肝细胞生成素已作为治疗各类慢性活动性肝炎、重症肝炎。肝硬化主要的治疗手段,在缓解和治疗急慢性肝坏死和改善严重肝功能障碍的病人方面,取得了比较满意的临床效果晗印。最近又有 研究 显示HGF有抗纤维化效应㈣,目前,促肝细胞生成素不仅广泛用于肝脏疾病及其相关症状的治疗,还能很好地保护和修复肝、肺、肾等器官的细胞,并促进器官和组织的再生和修复。此外,HGF对异源肿瘤细胞防止侵蚀或抑制增殖作用,促肝细胞生成素在胚胎肝脏和胎盘的发育中也有着显著的作用。随着人们对HGF日益引起的重视,促肝细胞生长素及其同类产品在临床上将具有广阔的应用前景。
尽管促肝细胞生长素及其他同类制剂具有多方面的生物效应,在临床上应用已比较成熟,但由于纯度原料及半成品标准不严,生产工艺没有统一的规程不能确保产品质量,纯度低、杂质含量高等不足,临床上也偶发头痛、发热、头晕等不良反应。另外, 研究 同时还发现高剂量的HGF能抑制人肝癌细胞的生长,小剂量则对人的某些肝癌细胞具有促进作用,所以存在着潜在用药剂量安全等问题。为了解决上述种种问题,改善目前的生产工艺条件,改善产品的质量迫在眉睫,从而保障临床应用安全的可靠性、疗效的有效性。
2、基因治疗方面
研究 主要集中在HGF基对肝细胞和组织的功能的影响,并主要以下两个方面进行了探索性 研究 和应用:首先是将表达HGF基因直接转入动物模型体内,使动物体合成较高水平的HGF,用于肝癌或肝硬化等的治疗。另外用HGF作为诱导,促进肝细胞增殖和分化,便于逆转录病毒载体或腺病毒载体介导的基因导入,提高基因治疗效率,在小鼠体内试验效果非常理想。目前国际上基因治疗已被高度重视,功能性表达基因体内转移载体和靶点导入给药途径的 研究 比较热门,靶向给药已成为世界性 研究 课题,肌注HGF已被动物实验证实是安全可行的提高肝内基因治疗效率有前途的方法。这给包括急慢性肝炎、肝硬化.肝切除手术的康复等等疾病的治疗带来了曙光。
免责申明:本文仅为中经纵横
市场
研究
观点,不代表其他任何投资依据或执行标准等相关行为。如有其他问题,敬请来电垂询:4008099707。特此说明。




